Publikacja artykułu w „Nature Communications” autorstwa naukowców z Wydziału Biologii UW dotycząca degradacji mRNA
20 10 2024
Naukowcy z Instytutu Genetyki i Biotechnologii Wydziału Biologii są wiodącymi autorami artykułu dotyczącego degradacji matrycowego RNA (mRNA), który został opublikowany na łamach „Nature Communications”. Naukowcy współpracowali z badaczami z Polskiej Akademii Nauk oraz Francis Crick Institute w Wielkiej Brytanii.
Autorami artykułu „Uridylation regulates mRNA decay directionality in fission yeast” są następujący naukowcy z Wydziału Biologii: Maciej Grochowski, dr inż. Lidia Lipińska -Zubrycka, dr Anna Golisz-Mocydlarz, dr Monika Zakrzewska-Płaczek, Borna Jurković oraz dr hab. Michał Małecki.
Badania prowadzone przez polsko-brytyjski zespół dotyczyły degradacji matrycowego RNA (mRNA). W komórkach eukariontów mRNA jest produkowane w jądrze, a następnie transportowane do cytoplazmy, gdzie służy jako szablon do produkcji białek, które realizują informacje zapisane w genomie. W cytoplazmie mRNA podlega ciągłej degradacji przez specjalne enzymy. Degradacja mRNA jest równie ważna jak jego produkcja w jądrze, a jego nietrwała natura jest kluczowa dla regulacji i szybkich zmian ilości mRNA, a co za tym idzie, białek kodowanych przez poszczególne geny.
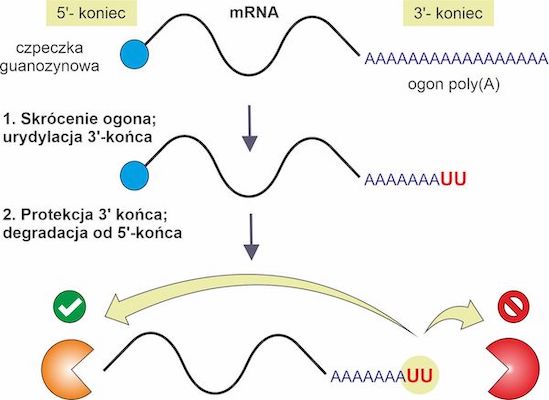
Degradacja mRNA jest procesem badanym od dawna i dobrze zrozumianym. W cytoplazmie mRNA jest stabilne, dopóki oba jego końce są chronione przed degradacją przez specjalne struktury. Na końcu 5’ znajduje się „czapeczka” utworzona z zmodyfikowanego nukleotydu guanyzowego, a na końcu 3’ długi „ogon” z około stu nukleotydów adenozynowych (ogon poliadenozynowy [poli(A)]). Degradacja mRNA zaczyna się od skrócenia ogona poli(A) do kilkunastu reszt adenozynowych. To prowadzi do aktywacji enzymów, które usuwają czapeczkę guanozynową i do degradacji mRNA przez egzonukleazę – enzym który usuwa pojedyncze nukleotydy od końca 5’ aż do całkowitego rozkładu cząsteczki mRNA. W cytoplazmie są także enzymy, które mogą degradować mRNA od końca 3’, jednak badania pokazują, że degradacja preferencyjnie zachodzi w jednym kierunku. Taki mechanizm pozwala na równoczesne występowanie translacji i degradacji tej samej cząsteczki mRNA. Mechanizmy regulujące kierunkowość degradacji nie są jednak dobrze poznane.
W pracy naukowcy pokazali, że dodatkowa modyfikacja 3’-końcowego ogona poliadenozynowego przez dodanie jednej lub kilku reszt urydynowych pomaga przekierować degradację na drugi koniec mRNA (koniec 5’). Uzyskane wyniki to efekt opracowania nowej techniki, która pozwala na badanie urydylacji w skali genomowej. Badania przeprowadzono używając organizmu modelowego – drożdży rozszczepkowych (Schizosaccharomyces pombe). Urydylacja jest rozpowszechniona w większości zbadanych organizmów eukariontów i autorzy publikacji postulują, że pełni tam podobną rolę w degradacji cytoplazmatycznego mRNA jak ta zaobserwowana u drożdży.
Ryc. Urydylacja 3′-końca reguluje kierunkowość degradacji mRNA
